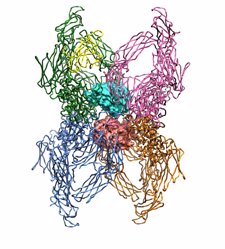
Foto: CSIC/EUROPA PRESS
MADRID, 10 Feb. (EUROPA PRESS) -
Un estudio internacional liderado por el Consejo Superior de Investigaciones Científicas (CSIC) ha desvelado, mediante cristalografía de rayos X, la estructura tridimensional de la proteina alfa2macroglobulina, inhibidor gigante que se encuentra en la sangre y es capaz de bloquear la acción de diversas proteinasas.
Las conclusiones de este estudio, publicado en el último número de la revista 'Angewandte Chemie', podrían ayudar en la investigación de enfermedades como el Alzheimer, el cáncer o el sida, ya que la alfa2-macroglobulina actúa como una trampa para las proteínas encargadas de cortar otras enzimas.
"El fallo en la regulación de las proteinasas puede dar lugar a procesos patológicos. El cáncer y la metástasis, el Alzheimer, las enfermedades cardiovasculares e inflamatorias, los procesos infecciosos por microorganismos, como la peste, el sida, el cólera, la malaria o la enfermedad de Chagas son algunos de los ejemplos de enfermedades que contemplan o se deben a la actuación nociva, errónea o descontrolada de proteinasas", explica el investigador del CSIC Francesc Xavier Gomis, del Instituto de Biología Molecular de Barcelona.
Respecto al hallazgo, el experto señala que lo novedoso de este inhibidor, que forma una gran cavidad central, "es que atrapa sus presas en su interior mediante un sofisticado mecanismo", algo que, añade, "recuerda al de las plantas carnívoras: un corte en una región anzuelo desencadena toda una serie de cambios a gran escala que hacen que la trampa se cierre y la proteinasa quede atrapada".
Una vez cerrada, los cambios estructurales en la partícula inhibidora hacen que sea reconocida por receptores extracelulares de varios tipos de células. Este hecho hace que se internalice y sea degradada por los lisosomas de la célula.
Una proteinasa es un enzima que corta otras proteínas, como las que tenemos en el tracto digestivo y que descomponen las proteínas que nos comemos. Unas participan en la complicada cascada de coagulación de la sangre y la fibrinólisis. Otras en emplean en remodelación de tejidos, como ocurre en procesos postmestruales, desarrollo embrionario, etc.
"Prácticamente no hay proceso biológico en el que no intervenga al menos una proteinasa. Como estas enzimas cortan otras proteínas, es muy importante que estén regulados de forma muy estricta y ahí es donde juegan un papel importantísimo los inhibidores", explica el investigador.
Los investigadores han llegado a sus resultados mediante la técnica experimental de la cristalografía de proteínas. Este método requiere la purificación y aislamiento de una proteína mediante técnicas cromatográficas. Una vez se ha obtenido la proteína pura, se cristaliza y los microcristales resultantes se analizan con radiación de rayos X, que permiten resolver la estructura tridimensional.